摘要
背景
姜黄素加速口腔伤口愈合;然而,负责任的机制仍未得到充分探讨。我们的假设是姜黄素在人牙龈成纤维细胞(hGFs)中调节伤口愈合相关基因的表达。本研究探讨了姜黄素是否能调节未损伤hGF中的转化生长因子(TGF)-β1、I型TGF-β受体(TGF-β ri)、II型TGF-β受体(TGF-β rii)和血管内皮生长因子(VEGF)的表达,以及体外hGF创面愈合模型。
方法
采用MTT法评价姜黄素的细胞毒性。用无细胞毒浓度的姜黄素处理未损伤的hGFs 24小时。通过定量聚合酶链式反应检测基因表达。然后,用1µM姜黄素在体外伤口愈合模型中处理hGFs。对PD98059进行预处理,以确定姜黄素调控基因表达是否需要细胞外信号调节激酶(ERK)信号通路。
结果
0.1 ~ 20 μ M的姜黄素对细胞活力无显著影响。在未损伤的hgf中,姜黄素对TGF-β1、TGF-βRI、TGF-βRII和VEGF表达无显著影响。相反,姜黄素在体外创面愈合模型中显著上调了这些基因的表达。PD98059显著降低了姜黄素刺激的TGF-βRI、TGF-βRII和VEGF的表达,而对TGF-β1的表达无影响。
结论
姜黄素在体外hGF创面愈合模型中上调TGF-β1、TGF-βRI、TGF-βRII和VEGF的表达。ERK通路是姜黄素诱导TGF-βRI、TGF-βRII和VEGF的必要途径。我们的研究结果支持姜黄素作为牙龈溃疡的治疗剂的发展。
背景
牙龈伤口愈合是一个复杂的过程,受多种细胞类型的信号调控,包括免疫细胞、成纤维细胞、内皮细胞和角质形成细胞[1].伤口愈合过程包括四个阶段:(1)止血,(2)炎症,(3)增生,(4)重塑[2].牙龈成纤维细胞通过分泌多种细胞因子、生长因子和细胞外基质,包括转化生长因子β (TGF-β)、血管内皮生长因子(VEGF)、表皮生长因子、成纤维细胞生长因子、胶原蛋白等,在伤口愈合的增殖期发挥重要作用[3.],这些都对伤口愈合至关重要[4].
TGF-β是其家族的原型细胞因子,由活化的巨噬细胞、血小板、角质形成细胞和成纤维细胞产生[5,6,7,8].细胞因子在调节多种细胞功能中发挥重要作用[9].具体而言,TGF-β1通过引发炎症、形成肉芽组织、刺激胶原蛋白合成和伤口收缩来促进伤口愈合[10,11,12].虽然三种TGF-β亚型(TGF-β1、TGF-β2和TGF-β3)在结构上有60% - 80%的相似性,但它们是由不同的基因编码的。这些异构体以非活性分子的形式分泌,在与它们的特定受体(I型TGF-β受体(TGF-β ri)和II型TGF-β受体(TGF-β rii)结合之前被激活[13].
VEGF家族包括VEGF- a、VEGF- b、VEGF- c、VEGF- d和胎盘生长因子[14].VEGF由血小板、中性粒细胞、内皮细胞、成纤维细胞和巨噬细胞产生[15,16,17,18,19].VEGF最初被认为是一种招募炎症细胞的血管通透性因子。VEGF在伤口愈合过程中上调[20.].VEGF通过刺激内皮细胞增殖和形成新血管,促进伤口愈合增殖期血管生成和肉芽组织形成[21].VEGF在炎症、再上皮化和瘢痕组织形成中也有重要作用[21].
姜黄素(diferuloylmethane),属于姜黄素家族,是姜黄根茎的主要成分,是姜黄呈黄色的原因[22].姜黄素长期以来一直被用作香料和草药[23].姜黄素具有抗菌、抗炎、抗氧化和抗癌的特性[24,25,26,27].在动物模型和临床研究中,姜黄素已被证明能刺激皮肤和口腔伤口愈合[28,29,30.,31,32].姜黄素促进大鼠真皮创面成纤维细胞增殖,提高抗氧化酶水平[28,31].此外,姜黄素促进了大鼠皮肤伤口中胶原蛋白的产生,并减少了基质金属蛋白酶-9的产生[32].姜黄素用于治疗兔口腔伤口时,可加速兔上唇牙龈黏膜溃疡的愈合[29].临床上,与安慰剂相比,外用姜黄素凝胶显著减小了轻度阿弗斯溃疡的大小[30.].虽然姜黄素已经证明了显著的伤口愈合特性,但在口腔伤口愈合过程中,细胞对姜黄素治疗的反应仍不清楚。
先前的研究发现,姜黄素通过调节酶活性和信号通路,如丝裂原活化蛋白激酶(MAPK),调控基因表达[33,34].然而,姜黄素对牙龈成纤维细胞基因表达的影响及其信号通路知之甚少。因此,我们利用体外人牙龈成纤维细胞(hGF)创面愈合模型,研究了姜黄素和细胞外信号调节激酶(ERK)抑制剂对TGF-β1、TGF-βRI、TGF-βRII和VEGF表达的影响。
方法
细胞培养
从三名供体的健康牙龈组织外植体中分离出hgf(两男一女;平均年龄,21.3岁),接受手术拔除第三磨牙。所有受试者均获得知情同意书。研究方案得到朱拉隆功大学牙科学院伦理委员会的批准。
hgf的分离如前所述[35].简单地说,外植体立即转移到含有10%胎牛血清(FBS, Gibco, Waltham, MA, USA)的Dulbecco 's Modified Eagle 's Medium (DMEM) (Sigma-Aldrich, St. Louis, MO, USA)的冰冷培养基中。收集的牙龈组织用磷酸盐缓冲盐水(PBS, Gibco)清洗。试样切成1mm2在含10% FBS的DMEM中培养,37℃,5% CO加湿2的气氛。实验中使用了第三至第五代的初级hgf。每个独立实验使用三个供体细胞系。
姜黄素的制备
姜黄素(Sigma-Aldrich)溶解在二甲基亚砜(DMSO, Sigma-Aldrich)中,根据制造商的说明,由于其在水中的溶解度非常低。所有实验中DMSO的最终浓度均为0.1%。
细胞活力测定
HGFs以5 × 10播种3.将细胞/孔置于96孔平底组织培养板中,在含10%胎牛血清的DMEM中培养24小时。将培养基替换为含0-50 μ M姜黄素(Sigma-Aldrich)的无血清DMEM,细胞再孵育24小时。使用MTT法测定细胞存活率。简单地说,除去培养基,在每个孔中加入100 μ L 0.7 mg/mL MTT (Invitrogen, Waltham, MA, USA)无血清DMEM溶液,并将板孵育90分钟,直到显微镜下可见甲醛晶体形成。在孵育期结束时,除去MTT溶液,将100µL二甲亚砜(DMSO, Sigma-Aldrich)加入孔中,轻轻混合以溶解甲醛晶体。用平板阅读器(EZ Read 400;Biochrom Cambridge,英国)570纳米。细胞存活率计算公式如下:
基因表达及qPCR分析
基因表达的测定如前所述[35].简单地说,hGFs以6 × 10播种5在含有10%胎牛血清的DMEM中,每60mm培养皿中有细胞。第二天,用PBS清洗细胞,用无血清DMEM替换培养基24小时。然后用0-20 μ M姜黄素孵育细胞24小时。然后,进行总RNA提取,并通过定量聚合酶链反应(qPCR)评估基因表达,如前所述[35].简单地说,提取总RNA,并从每个样品中逆转录2µg总RNA。cDNA模板扩增45个周期。qPCR引物见表1.每个反应进行两次。琼脂糖凝胶电泳和熔融曲线分析验证了PCR产物的特异性。将各基因的表达归一化为GAPDH的表达−ΔΔCt方法。每个图中显示的基因表达表示三个独立实验的平均值。首先对所有姜黄素剂量进行qPCR和基因表达分析,然后选择最有效的浓度进行伤口愈合模型分析。
体外创面愈合模型(划痕试验)
如前所述进行划痕试验[35,36].简单地说,将hgf种在含有10%胎牛血清的DMEM中60毫米的培养皿中。第二天,清洗细胞,用无血清dmem替换培养基24小时。接下来,使用无菌200 μ L移液管尖端在细胞单层上建立一条直线。然后去除培养基,细胞在含有DMSO或1 μ M姜黄素的培养基中孵育24小时。提取总RNA,通过qPCR检测基因表达。在ERK信号传导抑制剂实验中,细胞用DMSO或100 nM PD98059 (Cell signaling Technology, Danvers, USA)孵育1小时,然后DMSO或1µM姜黄素处理24小时。
统计分析
在每个实验条件下,数据以三个不同受试者的牙龈成纤维细胞的三个独立实验的均值±标准差表示(n = 9)。采用Shapiro-Wilk检验进行正态性检验。正态分布数据采用独立模型进行分析t-test或单向方差分析,然后是Tukey的诚实显著差异检验。p< 0.05为有统计学意义。
结果
姜黄素对hGF活力的影响
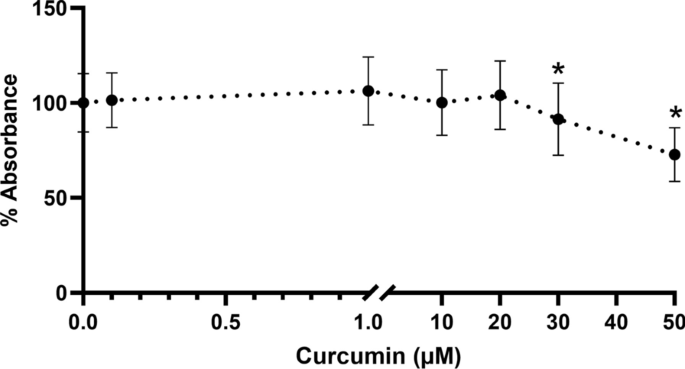
用MTT法评价姜黄素处理的HGFs的细胞活力。数字1表明0.1-20 μ M姜黄素不改变细胞活力,而30和50 μ M姜黄素显著诱导浓度依赖性细胞毒性(p< 0.05)。因此,在随后的实验中,姜黄素的浓度为0.1-20 μ M。
姜黄素对创面愈合相关基因表达的影响
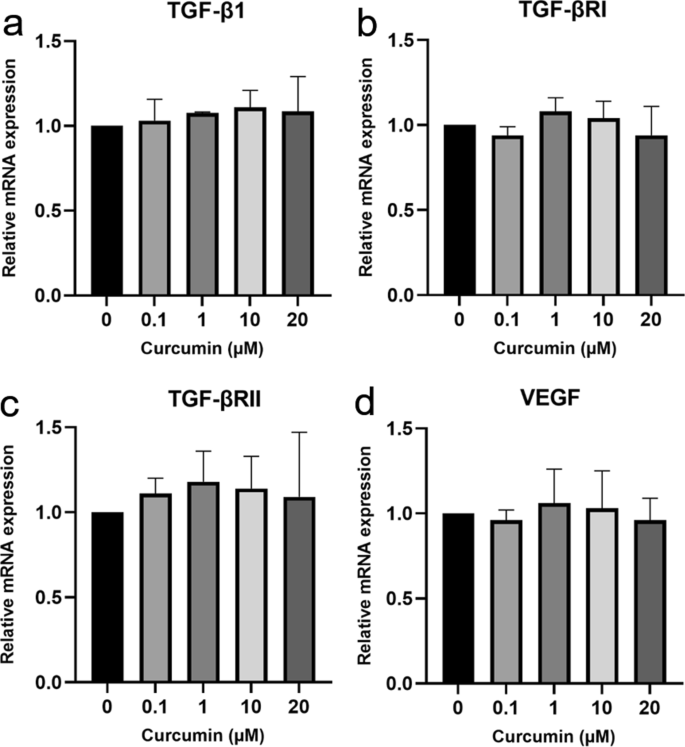
在未损伤的牙龈成纤维细胞中,0.1-20µM姜黄素对TGF-β1、TGF-βRI、TGF-βRII或VEGF表达无显著影响(图2)。2).然而,我们之前的研究发现1µM是诱导其他基因表达的最佳姜黄素浓度,如角化细胞生长因子-1和表皮生长因子受体。因此,我们在后续实验中使用了1µM姜黄素[35].
姜黄素诱导体外创面愈合模型中TGF-β1、TGF-β受体和VEGF表达
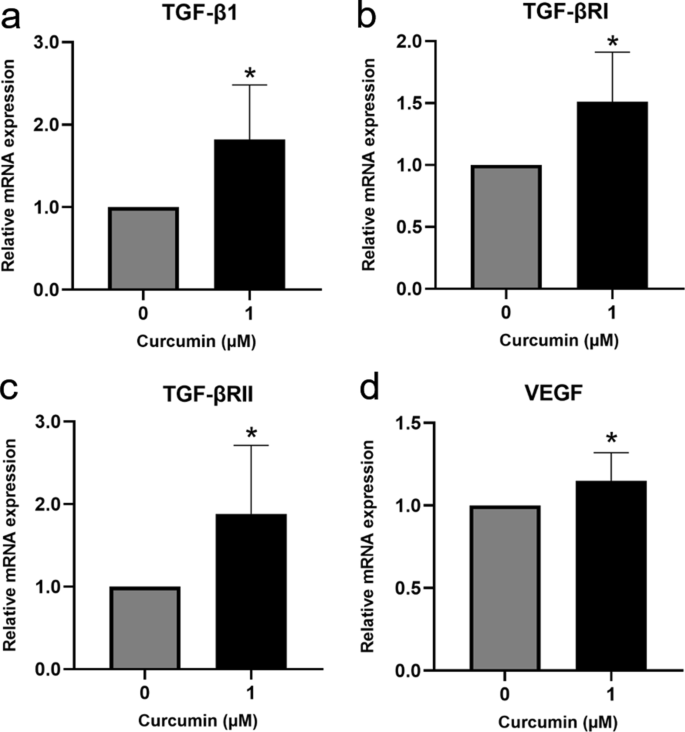
为了研究姜黄素在体外创面愈合模型中的作用,用hGF单层膜进行划伤实验,然后用1µM姜黄素处理24小时。姜黄素显著上调TGF-β1、TGF-βRI、TGF-βRII和VEGF mRNA表达(p在体外伤口愈合模型中,与载体处理的对照组相比,< 0.05)。3.).
ERK信号抑制降低了体外创面愈合模型中姜黄素刺激基因的表达
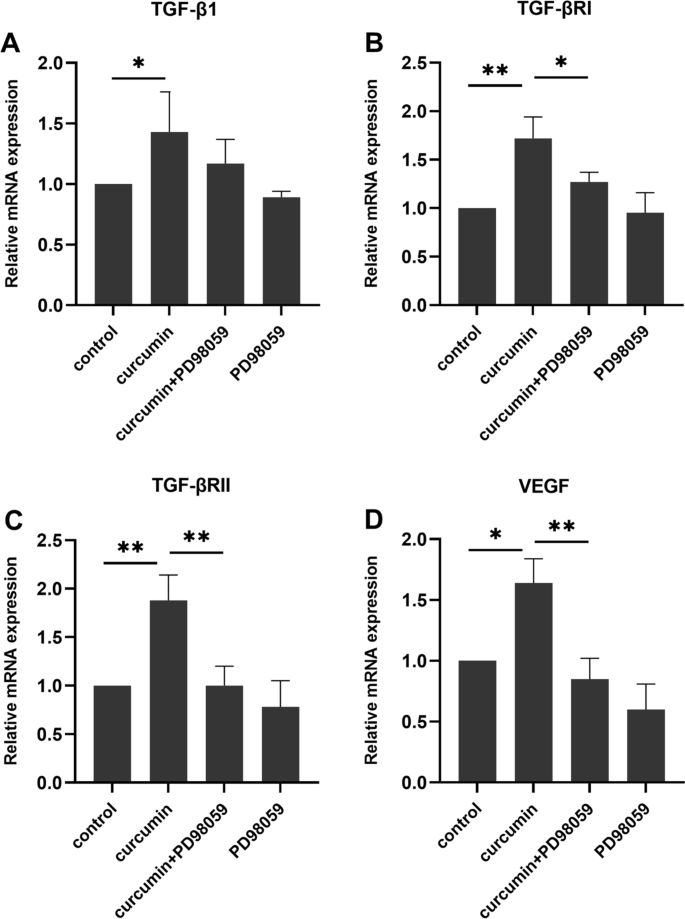
为了确定ERK信号是否参与姜黄素刺激的基因表达,在姜黄素处理之前,用PD98059培养损伤的hGF单层。PD98059对姜黄素诱导的TGF-β1表达无影响(图。4a).然而,PD98059显著降低了姜黄素诱导的TGF-βRI、TGF-βRII和VEGF mRNA的表达p< 0.05,图;4罪犯)。
讨论
在本研究中,我们首先研究了姜黄素对hGFs的细胞毒性。结果表明,0.1-20 μ M姜黄素对hGF活性无显著影响,而30-50 μ M姜黄素显著诱导浓度依赖性细胞毒性。然后,我们证明了姜黄素对未损伤的hgf中TGF-β1、TGF-βRI、TGF-βRII或VEGF mRNA的表达没有显著影响。有趣的是,在体外创面愈合模型中,姜黄素显著刺激了hgf中TGF-β1、TGF-βRI和TGF-βRII的表达。
既往研究报道TGF-β1在未愈合伤口中的表达明显低于正常愈合溃疡[37,38].此外,许多研究报告称,外源性TGF-β1治疗伤口可促进伤口愈合[39,40,41].TGF-β受体定位于多种细胞类型的细胞表面,包括成纤维细胞和内皮细胞[42,43].在以往的研究中,TGF-β受体在损伤后表达增加,损伤后第14天表达最高,到第56天表达下降[44].已有研究表明,姜黄素对TGF-β及其受体具有差异调控作用。具体而言,姜黄素在未受损和受损愈合皮肤伤口中诱导TGF-β1和TGF-βRII表达,而TGF-βRI仅在损伤后7天受损愈合伤口中表达增加[8].我们也报道了姜黄素对TGF-β及其受体的相似差异调控,姜黄素仅在体外伤口愈合模型中增加TGF-β及其受体的表达,而在未损伤的牙龈成纤维细胞中没有,支持姜黄素促进损伤组织愈合的概念[8].
VEGF是一种强烈的血管生成正调节因子,可刺激内皮细胞形成新血管[45].VEGF受体主要在内皮细胞上表达[46].由于血管密度降低,VEGF-A缺陷小鼠表现出延迟伤口闭合[47].在另一项研究中,姜黄素通过增加糖尿病大鼠肉芽组织中VEGF和TGF-β1的表达,促进血管形成和伤口愈合[48].除皮肤创面外,姜黄素还通过增加基质金属蛋白酶-2、TGF-β和VEGF的表达来促进吲哚美兴诱导的胃溃疡愈合[49].相应地,我们首次证明了姜黄素在体外hGF创面愈合模型中显著增加VEGF表达。然而,在未损伤的细胞单层中,VEGF的表达没有受到影响,这表明姜黄素以一种可控的“根据需要”的方式调节基因表达,因为VEGF的上调在未损伤的组织中是不必要的。然而,姜黄素在生理和损伤条件下差异调节基因表达的机制尚不清楚。
姜黄素部分通过调节MAPK的磷酸化活性来调控基因表达[33].MAPK通路在将细胞外信号转导为细胞反应中具有重要功能[50].MAPK家族包括MAPK(又称ERK)、C-Jun n端激酶/应激激活蛋白激酶和p38 MAPK [50].MAPK参与许多细胞功能,特别是调节细胞迁移和增殖[51,52].既往研究表明ERK信号通路通过促进角质形成细胞增殖和迁移,对皮肤伤口愈合的增殖期很重要[53].抑制ERK1/2或p38通路均可导致角膜上皮伤口愈合延迟[54].在本研究中,ERK信号抑制剂PD98059显著减弱了姜黄素刺激的TGF-βRI、TGF-βRII和VEGF的表达,而TGF-β1的表达不受影响。这些数据表明,姜黄素通过调节ERK通路,调节TGF-βRI、TGF-βRII和VEGF在hgf中的表达。我们的发现与我们之前的报告一致,姜黄素诱导的I型胶原蛋白和EGFR在hGFs中的表达也需要ERK激活[35].然而,以往的研究大多考察了姜黄素对各种癌细胞系的作用,并观察到姜黄素抑制ERK信号通路[33].综上所述,这些发现表明姜黄素可能在正常细胞和癌细胞中不同程度地调节ERK;然而,确切的机制需要进一步研究。
虽然本研究中使用的划痕试验并不是一个理想的伤口愈合模型,但它已被广泛用于研究许多药物和生物因素对角质形成细胞和成纤维细胞迁移的影响[36,55].在细胞水平上,抓挠诱导乳腺癌细胞中活性氧、Nrf2蛋白和应激反应基因的增加,包括热休克蛋白70和血红素氧合酶-1 [36].姜黄素的抗氧化特性可能会减少损伤细胞中ROS的产生,这可能是姜黄素促进伤口愈合的机制之一。需要进一步的研究来探索这种可能性。
抓挠引起的机械损伤会使受伤的细胞产生化学刺激,扩散到邻近的细胞。此外,抓挠引起损伤细胞内钙的增加,钙通过细胞-细胞连接传递到附近未受损的细胞。这种钙波传播到远离伤口边缘的细胞中[56].细胞内钙的增加会激活多种信号通路,导致基因表达的改变[57].这些数据表明,机械损伤不仅会改变伤口边缘细胞的基因表达,还会改变距离较远的细胞的基因表达。先前的研究表明,姜黄素剂量依赖性地降低结直肠癌细胞内钙水平[58].姜黄素是否能调节机械损伤引起的细胞内钙水平的变化,有待进一步研究。由于伤口愈合是一个复杂的过程,需要几种细胞类型之间的相互作用,因此使用一种细胞类型的划痕试验仅模拟对这些细胞的机械损伤。由于这一局限性,我们需要进一步的研究来支持我们在伤口愈合模型中姜黄素对基因表达的影响。
结论
在体外hGF创面愈合模型中,姜黄素显著上调TGF-β1、TGF-βRI、TGF-βRII和VEGF mRNA表达。ERK通路对于姜黄素刺激的TGF-βRI、TGF-βRII和VEGF mRNA表达至关重要。需要进一步研究姜黄素促进牙龈伤口愈合的其他机制。我们的研究结果支持姜黄素作为一种治疗牙龈溃疡的伤口愈合剂的治疗潜力。
数据和材料的可用性
在当前研究中生成和/或分析的数据集可以在Figshare存储库中获得,https://doi.org/10.6084/m9.figshare.15073029.
缩写
- hgf:
-
人类牙龈成纤维细胞
- 转化生长因子-β1:
-
转化生长因子1
- TGF -βRI:
-
I型TGF-β受体
- TGF -βRII:
-
II型TGF-β受体
- VEGF:
-
血管内皮生长因子
- 麻省理工:
-
(3 - (4, 5-Dimethylthiazol-2-yl) 2, 5-diphenyltetrazolium溴化)
- 兵:
-
细胞外信号调节激酶
- MAPK:
-
丝裂原活化蛋白激酶
- DMEM:
-
Dulbecco 's Modified Eagle 's medium
- 的边后卫:
-
胎牛血清
- PBS:
-
磷酸盐
- DMSO溶液:
-
二甲亚砜
- GAPDH:
-
Glyceraldehyde-3-phosphate脱氢酶
参考文献
- 1.
pasar I, Stojadinovic O, Yin NC, Ramirez H, Nusbaum AG, Sawaya A, Patel SB, Khalid L, Isseroff RR, Tomic-Canic M.伤口愈合中的上皮细胞:综合综述。中华外科杂志。2014;3(7):445-64。
- 2.
Diegelmann RF, Evans MC.伤口愈合:急性、纤维化和延迟愈合概述。《中国生物科学》2004;9:489 - 489。
- 3.
伤口愈合生物学。Periodontol。2000;22(1):44-50。
- 4.
Barrientos S, Stojadinovic O, Golinko MS, Brem H, Tomic-Canic M.生长因子和细胞因子在伤口愈合中的作用。创伤修复再生。2008;16(5):585-601。
- 5.
李世峰,李志强,李志强,李志强。UVB对人角质形成细胞tgf - β 1生成的调控。中华皮肤医学杂志,1997;6(2):105-10。
- 6.
Eppley BL, Woodell JE, Higgins J.从富血小板血浆中血小板定量和生长因子分析:伤口愈合的意义。中华整形外科杂志,2004;29(6):344 - 344。
- 7.
吴玲,俞yl, Galiano RD, Roth SI, Mustoe TA。巨噬细胞集落刺激因子通过组织巨噬细胞加速伤口愈合,上调TGF-beta1 mRNA水平。中华外科杂志,2001;29(2):344 - 344。
- 8.
Mani H, Sidhu GS, Kumari R, Gaddipati JP, Seth P, Maheshwari RK。姜黄素在伤口愈合受损过程中差异调节TGF-beta1及其受体和一氧化氮合酶。BioFactors(牛津,英国)。2002; 16(1 - 2): 29-43。
- 9.
Tirado-Rodriguez B, Ortega E. TGF-β:过敏性疾病的重要介质和在癌症发展中具有双重活性的分子。中华免疫杂志2014;2014:318481。
- 10.
彭丽丽,张志刚,张志刚。生长因子β在不同创面愈合过程中的作用。中华外科杂志。2013;2(5):215-24。
- 11.
转化生长因子β通过成纤维细胞刺激胶原基质收缩:对伤口愈合的影响。美国国家科学研究院。1988; 85(13): 4894 - 7。
- 12.
Desmouliere A, Geinoz A, Gabbiani F, Gabbiani G.转化生长因子- β 1在肉芽组织肌成纤维细胞和静止和生长的培养成纤维细胞中诱导α -平滑肌肌动蛋白的表达。中国生物医学工程学报,2001;29(1):344 - 344。
- 13.
克拉斯BR,格罗贝拉AO,罗尔夫KJ。转化生长因子beta1信号,伤口愈合和修复:一种具有临床意义的多功能细胞因子,对伤口修复,一个微妙的平衡。中华医学杂志(英文版);2009;29(5):344 - 344。
- 14.
沙利斯托,谭梅拉,法克奇拉,卡卡宁,苏米宁,伊拉-赫图阿拉,阿利塔洛,血管内皮生长因子c促进糖尿病伤口愈合。中华病理学杂志。2006;69(3):1080-7。
- 15.
Namiki A, Brogi E, Kearney M, Kim EA, Wu T, Couffinhal T, vararticovski L, Isner JM。缺氧诱导体外培养的人内皮细胞血管内皮生长因子。中国生物医学工程学报,2001;29(4):489 - 497。
- 16.
Detsch R, Stoor P, Grunewald A, Roether JA, Lindfors NC, Boccaccini AR.生物活性玻璃S53P4增加人成纤维细胞的VEGF分泌,刺激骨血管生成。中国生物医学工程学报,2014;29(4):344 - 344。
- 17.
Banks RE, Forbes MA, Kinsey SE, Stanley A, Ingham E, Walters C, Selby PJ。血小板中血管生成细胞因子血管内皮生长因子(VEGF)的释放:VEGF测量和癌症生物学的意义中华肿瘤学杂志,1998;37(6):366 - 366。
- 18.
王晓明,王晓明,王晓明,王晓明,王晓明。中性粒细胞细胞内血管内皮生长因子的研究进展。血。1997;90(10):4153 - 61。
- 19.
Berse B, Brown LF, Van de Water L, Dvorak HF, Senger DR.血管通透性因子(血管内皮生长因子)基因在正常组织、巨噬细胞和肿瘤中表达差异。Mol生物细胞。1992;3(2):211-20。
- 20.
Brown LF, Yeo KT, Berse B, Yeo TK, Senger DR, Dvorakvan de Water HFL。伤口愈合过程中表皮角质形成细胞血管通透性因子(血管内皮生长因子)的表达。中华检验医学杂志,2002,19(3):344 - 344。
- 21.
鲍P, Kodra A, Tomic-Canic M, Golinko MS, Ehrlich HP, Brem H.血管内皮生长因子在伤口愈合中的作用。中华外科杂志,2009;32(2):347-58。
- 22.
Sharma RA, Euden SA, Platton SL, Cooke DN, Shafayat A, Hewitt HR, Marczylo TH, Morgan B, Hemingway D, Plummer SM,等。口服姜黄素的I期临床试验:系统活性和依从性的生物标志物。临床肿瘤学杂志,2004;10(20):6847-54。
- 23.
查托帕德哈伊I,比斯瓦斯K,班约帕德哈伊U,班纳吉RK。姜黄和姜黄素:生物作用和药用应用。中国科学(d辑),2004;
- 24.
梁刚,杨松,周浩,邵玲,黄凯,肖军,黄忠,李霞。姜黄素类似物的合成、晶体结构及抗炎性能。中华医学杂志2009;44(2):915-9。
- 25.
李娟,曹慧。姜黄素对糖尿病及其并发症的抗氧化和抗炎作用。中国医药杂志,2013;19(11):2101-13。
- 26.
姜黄素I的抑菌活性与细菌膜损伤有关。PLoS ONE。2015; 10 (3): e0121313。
- 27.
Aggarwal S, Takada Y, Singh S, Myers JN, Aggarwal BB。姜黄素通过调节核因子- kappab信号通路抑制人头颈部鳞状细胞癌细胞的生长和存活中华癌症杂志,2004;11(5):679-92。
- 28.
Akbik D, Ghadiri M, Chrzanowski W, Rohanizadeh R.姜黄素作为伤口愈合剂。中国生物医学工程学报,2014;26(1):1 - 7。
- 29.
林玉生,权SK,朴志华,赵昌昌,朴文寿,金威。姜黄素促进口腔溃疡模型动物黏膜愈合。喉镜。2016;126 (2):e68 - 73。
- 30.
姜黄素凝胶治疗轻度阿弗他溃疡:一项随机、安慰剂对照试验。中国医学植物学报,2012;1(41):40-5。
- 31.
戈皮纳斯D,艾哈迈德先生,戈马提K, Chitra K, Sehgal PK, Jayakumar R.皮肤伤口愈合过程与姜黄素胶原蛋白膜。生物材料。2004;25(10):1911 - 7。
- 32.
Bhagavathula N, Warner RL, DaSilva M, McClintock SD, Barron A, Aslam MN, Johnson KJ, Varani J.姜黄素和生姜提取物的组合促进皮质激素损伤无毛大鼠皮肤擦伤愈合。创伤修复再生。2009;17(3):360-6。
- 33.
姜黄素作用的分子机制:基因表达。BioFactors。2013年,39(1):37-55。
- 34.
方刚,陈松,黄强,陈玲,廖东。姜黄素通过抑制p38 MAPK/ERK信号通路调控心肌成纤维细胞增殖和细胞周期,抑制心肌成纤维细胞活性。Mol Med rep 2018;18(2): 1433-8。
- 35.
姜黄素促进I型胶原蛋白、角化细胞生长因子-1和表皮生长因子受体在人牙龈成纤维细胞体外伤口愈合模型中的表达。中国生物医学工程学报。2011;15(1):63-70。
- 36.
李亚希,杨勇,张德东,张德明,王pk。损伤诱导的细胞集体迁移的单细胞基因表达分析。整合生物学(Camb)。2014; 6(2): 192 - 202。
- 37.
Cowin AJ, Hatzirodos N, Holding CA, Dunaiski V, Harries RH, Rayner TE, Fitridge R, Cooter RD, Schultz GS, Belford DA。愈合对腿慢性静脉性溃疡中转化生长因子及其受体表达的影响。中华皮肤病学杂志。2001;17(5):1282-9。
- 38.
Jude EB, Blakytny R, Bulmer J, Boulton AJ, Ferguson MW。转化生长因子- 1、2、3和受体I型和II在糖尿病足溃疡中的作用。中华医学会糖尿病杂志2002;19(6):440-7。
- 39.
Quaglino D Jr, Nanney LB, Ditesheim JA, Davidson JM。转化生长因子- β刺激伤口愈合和调节猪皮细胞外基质基因表达:切口伤口模型。中华皮肤病学杂志。1991;97(1):34-42。
- 40.
Quaglino D Jr, Nanney LB, Kennedy R, Davidson JM。转化生长因子- β刺激伤口愈合和调节猪皮肤细胞外基质基因表达。一、切口模型。实验室调查技术方法病原学杂志,1990;63(3):307-19。
- 41.
Mustoe TA, Pierce GF, Thomason A, Gramates P, Sporn MB, Deuel TF。转化生长因子- β诱导大鼠切口伤口加速愈合。科学。1987;237(4820):1333 - 6。
- 42.
Goumans MJ, Valdimarsdottir G, Itoh S, Lebrin F, Larsson J, Mummery C, Karlsson S, ten Dijke p激活素受体样激酶(Activin receptor-like kinase, ALK)1是TGFbeta/ALK5信号通路的拮抗介质。生物化学学报,2003;12(4):817-28。
- 43.
Petridou S, Maltseva O, Spanakis S, Masur SK. tgf - β受体表达和smad2定位在成纤维细胞中是细胞密度依赖的。中华眼科杂志2000;41(1):89-95。
- 44.
杨晓明,张晓明,张晓明,等。转化生长因子- β受体在兔屈肌腱损伤愈合模型中的表达。中华整形外科杂志,2001;26(5):457 - 457。
- 45.
梁德伟,邝文杰,郭德尔DV,费ara N.血管内皮生长因子是一种分泌性血管生成有丝分裂原。科学。1989;246(4935):1306 - 9。
- 46.
张志刚,张志刚,张志刚。甲状腺疾病中血管内皮生长因子(VEGF)、VEGF受体表达与微血管密度的关系。中华实用医学杂志,2007;29(4):344 - 344。
- 47.
罗思德,张志刚,张志刚,张志刚,张志刚。血管内皮生长因子a在小鼠表皮角质形成细胞中的作用及其对肿瘤形成的影响。癌症杂志2004;64(10):3508-16。
- 48.
姜黄素诱导血管新生促进糖尿病大鼠创面愈合的研究。中华外科杂志,2015;29(2):344 - 344。
- 49.
沙玛AV, Ganguly K, Paul S, Maulik N, Swarnakar S.姜黄素通过VEGF和MMP-2介导的信号通路刺激血管生成和胶原纤维的恢复来治疗吲哚美酸诱导的胃溃疡。抗氧化氧化还原信号。2012;16(4):351-62。
- 50.
张伟,刘海涛。MAPK信号通路在哺乳动物细胞增殖调控中的作用。Cell res 2002;12(1): 9-18。
- 51.
何敏,薛志明,李娟,周伯强。灯盏花素通过抑制ERK1/2 MAPK信号通路抑制高糖诱导的大鼠血管平滑肌细胞增殖和迁移。药物学报。2012;33(5):606-14。
- 52.
Klemke RL, Cai S, Giannini AL, Gallagher PJ, de Lanerolle P, Cheresh DA。丝裂原活化蛋白激酶对细胞运动的调节。中国生物医学工程学报,2001;26(2):344 - 344。
- 53.
Shibata S, Tada Y, Asano Y, Hau CS, Kato T, Saeki H, Yamauchi T, Kubota N, Kadowaki T, Sato S.脂联素通过ERK信号通路促进角质形成细胞增殖和迁移调节皮肤伤口愈合。J免疫(巴尔的摩,马里兰州:1950年)。2012年,189(6):3231 - 41。
- 54.
沙玛GD,何杰,巴赞He。p38和ERK1/2在上皮性伤口愈合中协调细胞迁移和增殖:MAP激酶级联之间的串音激活的证据。中国生物医学工程学报,2003;29(4):489 - 497。
- 55.
李志强,李志强,李志强,等。牙龈创面愈合的细胞生物学研究。Periodontol。2000;24:127-52。
- 56.
Sammak PJ, Hinman LE, Tran POT, Sjaastad MD, Machen TE。受损细胞如何与存活的细胞单层通信?中国生物医学工程学报,1997;29(2):344 - 344。
- 57.
Ghilardi SJ, O 'Reilly BM, Sgro AE。细胞内信号动力学及其在协调组织修复中的作用。威利跨学科Rev Syst生物医学2020;12(3):e1479。
- 58.
陈玉春,郭涛,林绍善,林俊杰。姜黄素调节Ca(+2)离子和细胞p53蛋白诱导结直肠癌细胞HSP70基因表达Mol Carcinog. 1996;17(4): 224-34。
确认
作者感谢凯文·汤普金斯博士在审阅手稿时的协助。
资金
这项研究得到了泰国国家研究委员会2018年研究生研究基金的支持,该基金在研究的设计、数据的收集、分析和解释或撰写手稿方面没有任何作用。
作者信息
从属关系
贡献
AR有助于研究概念化、数据采集、统计分析和原始草案的准备。SS在研究概念化、数据解读、审稿和编辑等方面做出了贡献。两位作者都阅读并批准了最终的手稿。
相应的作者
道德声明
伦理批准并同意参与
在涉及人类参与者的研究中进行的所有程序都符合朱拉隆功大学牙科学院伦理委员会的道德标准。研究中所有个体参与者都获得了知情同意。
发表同意书
不适用。
相互竞争的利益
作者宣称他们之间没有利益冲突。
额外的信息
出版商的注意
施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条所提供的资料,除非在资料的信用额度中另有说明。
关于本文
引用本文
Rujirachotiwat, A., Suttamanatwong, S.姜黄素在体外人牙龈成纤维细胞伤口愈合模型中上调转化生长因子-β1及其受体和血管内皮生长因子的表达。BMC口腔健康21,535(2021)。https://doi.org/10.1186/s12903-021-01890-9
收到了:
接受:
发表:
关键字
- 姜黄素
- 齿龈
- 成纤维细胞
- 伤口愈合
- 血管内皮生长因子
- 转化生长因子